处方药 利多卡因贴片 利多卡因贴片经美国食品及药物管理局批准用于特定病症,主要是带状疱疹后遗神经痛(PHN),这是一种带状疱疹后的持续性神经痛并发症。虽然研究表明这种药物有可能用于其他神经病理性疼痛和肌肉骨骼疼痛,但 FDA 的正式批准仍仅限于 PHN。这些贴片通过阻断浅表神经纤维中的钠通道提供局部缓解,使其成为某些类型慢性疼痛的针对性选择。
要点说明:
-
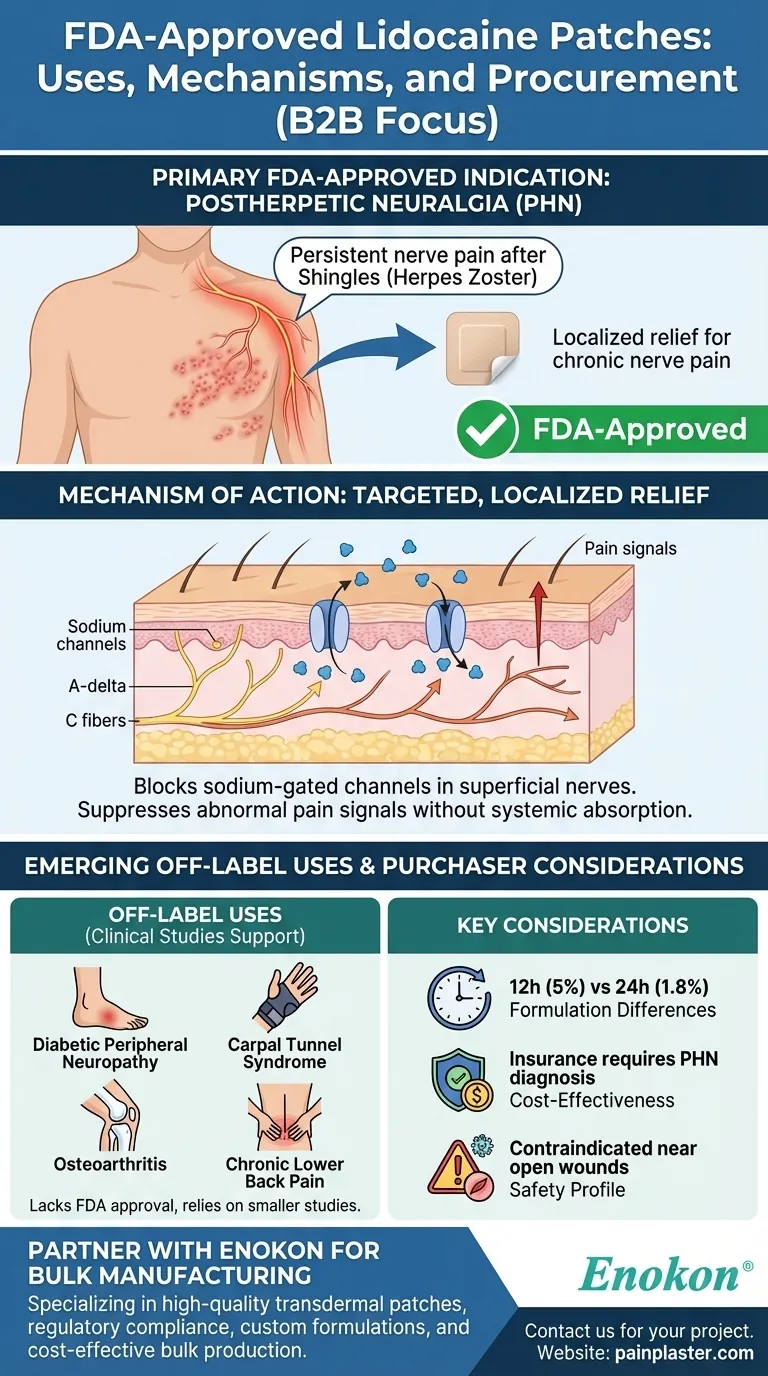
FDA 批准的主要适应症:带状疱疹后神经痛 (PHN)
- 带状疱疹是一种由带状疱疹(带状疱疹感染)后神经损伤引起的慢性疼痛,美国食品及药物管理局已批准 5%和 1.8%处方利多卡因贴片专门用于治疗带状疱疹后神经痛。
- PHN 表现为以前受带状疱疹皮疹影响的部位出现烧灼感、刺痛或过敏,通常持续数月至数年。
-
作用机制
- 利多卡因贴片通过阻断皮下局部 A-delta 和 C 神经纤维中的钠门控通道发挥作用。
- 这种作用可抑制异常疼痛信号,而不会被全身吸收,与口服药物相比,可将副作用降至最低。
-
有研究支持的标示外用途 虽然尚未获得美国食品及药物管理局的批准,但临床研究表明它对以下方面具有疗效
- 糖尿病周围神经病变:糖尿病导致的神经损伤引起的疼痛。
- 腕管综合征:正中神经压迫性神经病。
- 骨关节炎:关节疼痛,尤其是膝盖等浅表部位。
- 慢性下背痛:特别是当存在神经病理性成分时。
-
购买者注意事项
- 配方差异:5%的贴片(如 Lidoderm)每天可贴 12 小时,而 1.8% 的贴片(如 ZTlido)由于粘附性更强,可贴 24 小时。
- 成本效益:保险通常要求 PHN 诊断;标示外使用可能需要事先授权。
- 安全性简介:开放性伤口或感染附近禁用;药物相互作用极小,适合老年患者使用。
-
监管背景
- 美国食品和药物管理局(FDA)的批准是基于严格的 PHN 专项试验,试验结果表明,从统计学角度看,疼痛减轻效果显著。
- 标示外应用则依赖于较小规模的研究或临床医生的经验,缺乏同等水平的监管审查。
对于医疗采购人员来说,了解这些区别可确保做出适当的采购和处方决策,平衡已获批准的适应症和其他疼痛综合征的新证据。

汇总表:
| 主要方面 | 详细信息 |
|---|---|
| FDA 批准的用途 | 带状疱疹后神经痛(PHN)--带状疱疹后的慢性神经痛。 |
| 作用机制 | 阻断浅表神经的钠通道,缓解局部疼痛。 |
| 标签外用途 | 糖尿病神经病变、腕管综合征、骨关节炎、慢性背痛。 |
| 配方选择 | 5%(12 小时涂抹)或 1.8%(24 小时涂抹)贴片。 |
| 安全性和保险范围 | 全身吸收最少;保险通常要求 PHN 诊断。 |
您的医疗机构或品牌需要可靠的、符合 FDA 标准的利多卡因贴片吗?
在 伊诺康 我们专业批量生产高品质透皮贴片,包括处方级止痛解决方案。我们的专业技术可确保
- 符合法规要求 满足 PHN 治疗和其他疼痛管理需求
- 定制配方 满足您的特殊要求
- 经济高效的批量生产 针对分销商和保健品牌
立即联系我们的团队 讨论您的利多卡因贴片采购或定制开发项目。
图解指南